 更多“原子序数为33的元素,其原子在n=4,l =1,m=0轨道中…”相关的问题
更多“原子序数为33的元素,其原子在n=4,l =1,m=0轨道中…”相关的问题
A.砷元素的最高正化合价为+3
B.砷元素是第4周期的主族元素
C.砷原子的第K电子层上有8个电子
D.砷的氧化物的水溶液呈强碱性
A.在周期表中,主族元素所在的族序数等于原子核外电子数
B.在周期表中,元素所在的周期序数等于原子核外电子层数
C.最外层电子数为8的粒子是稀有气体元素的原子
D.元素的原子序数越大,其原子半径也越大
(1)A的元素符号为(),其在元素周期表的位置:第()周期,第()族。
(2)元素A、B形成的最简单的气态氢化物稳定性较强的是()(填化学式),元素C和D可形成化合物DC2,其电子式为()。
(3)F的单质加入到D的最高价氧化物对应水化物的溶液中,发生反应的离子方程式为();上述反应的气体产物和C元素的单质设计成的燃料电池已用于航天飞机。试写出以30%KOH溶液为电解质溶液的这种电池在工作时负极的电极反应式为()。
(4)工业制取E的化学反应方程式为()。
下表是元素周期表中的部分元素的一些信息,请据表回答问题:
(1)氯原子的质子数是(),它属于()(填“金属”或“非金属”)元素。
(2)原子序数为3的元素与第三周期中的()(填名称)元素具有相似的化学性质,在化学反应中都比较容易()(填“得到”或“失去”)电子。
(3)写出原子序数为3的元素形成的氧化物的化学式()。
(4)根据表中信息查找规律,写出20号元素的原子结构示意图()。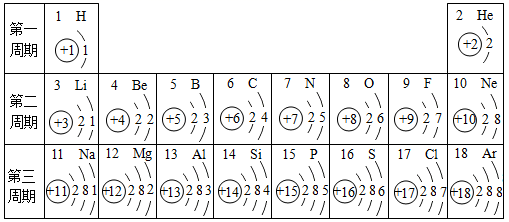
A.简单离子的还原性W>Y
B.X和R形成的化合物可以是离子化合物也可以是共价化合物
C.标况下,1molYZ与0.5molZ2混合后所得的气体的物质的量等于1mol
D.常温下,由X、Z、W形成的酸的浓度为0.1mol/L时,其pH>1
X、Y、Z、R为前四周期原子序数依次增大的元素。X原子有3个能级,且每个能级上的电子数相等;Z原子的不成对电子数在同周期中最多,且Z的气态氢化物在同主族元素的氢化物中沸点最低;X、Y、R三元素在周期表中同族。
(1)R元素基态原子的价层电子排布式为()。
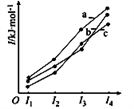
(2)下图表示X、Y、Z的四级电离能变化趋势,其中表示Y的曲线是()(填标号)。
 (3)化合物(XH2=X=O)分子中X原子杂化轨道类型分别是(),1mol(X2H5O)3Z=O分子中含有的σ键与π键的数目比为()。
(3)化合物(XH2=X=O)分子中X原子杂化轨道类型分别是(),1mol(X2H5O)3Z=O分子中含有的σ键与π键的数目比为()。
(4)Z与氯气反应可生成一种各原子均满足8电子稳定结构的化合物,其分子的空间构型为()。
(5)某R的氧化物立方晶胞结构如图所示,该物质的化学式为()。(用元素符号表示),已知该晶体密度为ρg/cm3,距离最近的原子间距离为dpm,则R的相对原子质量为()。(阿伏加德罗常数为NA)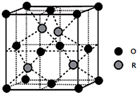
A.同周期元素中X的金属性最强
B.原子半径X>Y,离子半径X+>Z2-
C.同族元素中Z的氢化物稳定性最高
D.同周期元素中Y的最高价含氧酸的酸性最强
随原子序数递增,八种短周期元素(用字母X等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。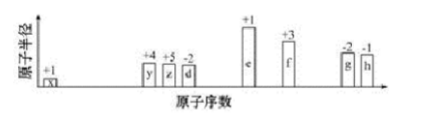 根据判断出的元素回答问题:
根据判断出的元素回答问题:
1)f在周期表中的位置是()。
2)比较d,e常见离子的半径大小(用化学式表示,下同):()>():比较g,h的最高价氧化物对应水化物的酸性强弱()>()。
3)任选上述元素组成一种四原子共价化合物,写出其电子式:()。
4)写出e的单质在足量d2中燃烧后的产物与y的高价氧化物反应的化学方程式()。
5)写出由x,y,z,d四种元素构成的离子化合物的化学式(写一种)()。
A.若X、Y原子序数相差l,Y为IIA族,则X一定是IIIA族
B.若Y(OH)m易溶于水,则X(OH)n一定不溶于水
C.若HnXOm为强酸,则X的氢化物溶液于水一定显酸性
D.若Y元素形成的单质是气体,则X元素形成的单质一定也是气体


 如果结果不匹配,请
如果结果不匹配,请 

















