 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
物质A的分解反应为一级反应,300K下经历了3600秒后,消耗掉A的量为75%,试求该一级反应的速率常数k=?反应的半衰期t1/2=?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“物质A的分解反应为一级反应,300K下经历了3600秒后,消…”相关的问题
更多“物质A的分解反应为一级反应,300K下经历了3600秒后,消…”相关的问题
双光气分解反应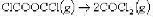 为一级反应。将一定量双光气迅速引入一个280°C的容器中,751s后测得系统的压力为2.710kPa;经过长时间反应完了后系统压力为4.008kPa。305°C时重复试验,经320s系统压力为2.838kPa;反应完了后系统压力为3.554kPa。求活化能。
为一级反应。将一定量双光气迅速引入一个280°C的容器中,751s后测得系统的压力为2.710kPa;经过长时间反应完了后系统压力为4.008kPa。305°C时重复试验,经320s系统压力为2.838kPa;反应完了后系统压力为3.554kPa。求活化能。
关于膨胀因子与膨胀率的概念
某气相一级分解反应A→3P,反应为一级,在等温的管式实验反应器中进行,加入原料为含A50%,含惰性物料50%。停留时间为10min,系统出口的体积的流量变为原来的1.5倍,求此时A的转化率及该反应在实验反应条件下的反应速率常数。
最近科学家提出“绿色自由”设想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。“绿色自由”设想技术流程如下
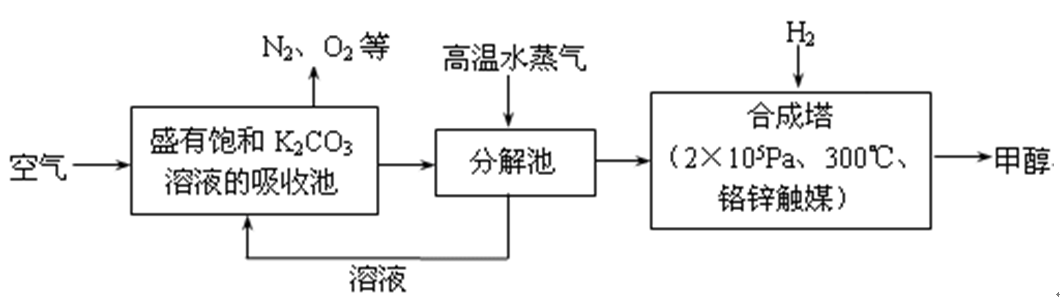
问题一、分解池中发生分解反应的物质是()。
问题二、在合成塔中,假设有CO2与足量H2kJ的热量,试写出合成塔中发生反应的热化学方程式()
问题三、①从平衡移动原理分析,低温有利于原料气的转化,而实际生产中采用300℃的温度,原因之一是考虑到催化剂的催化活性,原因之二是()。
②“绿色自由”设想技术流程中常包括物质和能量的“循环利用”,上述流程中能表达“循环利用”的除碳酸钾溶液外,还包括()。
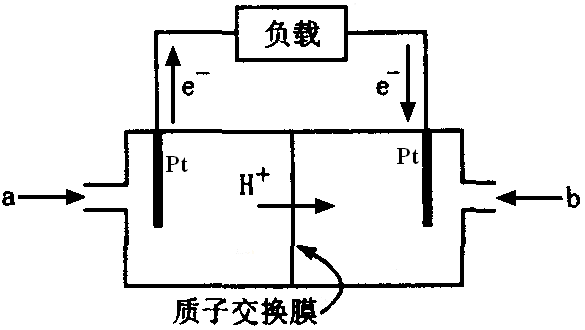
问题四、右图是甲醇燃料电池的结构示意图。已知电池总反应为:2CH3OH+3O2=2CO2+4H2O。通入a一端的电极是(填“正极”或“负极”),负极发生的电极反应是()。
 答案:
答案:
如图是2004年批量产生的笔记本电脑所用甲醇燃料电池的结构示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2═2CO2+4H2O2。下列说法正确的是()。
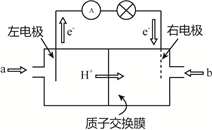
A.左电极为电池的正极,a处通入的物质是甲醇
B.右电极为电池的负极,b处通入的物质的空气
C.负极反应式为:CH3OH+H2O-6e-═CO2↑+6H+
D.正极反应式为:O2+2H2O+4e-═4OH-
NH3的分解反应为2NH3(g) N2(g)+3H2(g),在673K和100kPa总压下NH3(g)的解离度为98%,求该温度下反应的
N2(g)+3H2(g),在673K和100kPa总压下NH3(g)的解离度为98%,求该温度下反应的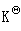 。
。
环氧乙烷的热分解是一级反应:C2H4O→CH4+CO在377℃时的半衰期为363min。 (1)在377℃时C2H4O分解掉99%需要多少时间? (2)若原来C2H4O为1mol,377℃经10h,生成CH4多少? (3)若此反应在417℃时半衰期为26.3min,求反应的活化能。
乙酸的水解反应可以近似看作一级反应,该反应在300K时的速率方程为:-rA(mol•m-3•s-1)=2.77×10-3cA。将乙酸浓度为600mol/m3的液体以0.05m3/min的速度送入一完全混合流反应器。试求以下几种情况下的乙酸的转化率:
问题一、反应器的体积为0.80m3时;
问题二、0.40m3的反应器,2个串联使用时;
问题三、0.20m3的反应器,4个串联使用时。
电池Ag(s)|AgCl(s)|KCl(m)|Hg2Cl2(s)|Hg(l)的电池反应为 Ag(s)+
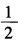 Hg2Cl2(s)→Agcl(s)+Hg(l) 已知298K时,此电池反应的焓变△rHm为5435J/mol,各物质的规定熵数据为 物质 Ag(s) AgCl(s) Hg(1) Hg2Cl2(s) SmΘ/(J/K.mol) 42.7 96.2 77.4 195.6 试计算该温度下电池的电动势E及电池电动势的温度系数
Hg2Cl2(s)→Agcl(s)+Hg(l) 已知298K时,此电池反应的焓变△rHm为5435J/mol,各物质的规定熵数据为 物质 Ag(s) AgCl(s) Hg(1) Hg2Cl2(s) SmΘ/(J/K.mol) 42.7 96.2 77.4 195.6 试计算该温度下电池的电动势E及电池电动势的温度系数
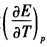 。
。
 试确定反应的速率方程式,并据此提出合理的反应机理(假设N2O5→N2O5+O2反应为控制步骤).
试确定反应的速率方程式,并据此提出合理的反应机理(假设N2O5→N2O5+O2反应为控制步骤).