题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
根据德拜-休克尔极限定律,计算298K时0.005mol/kg的CaCl2水溶液中Ca2+和Cl-的活度系数和离子平均活度系数。
根据德拜-休克尔极限定律,计算298K时0.005mol/kg的CaCl2水溶液中Ca2+和Cl-的活度系数和离子平均活度系数。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据德拜-休克尔极限定律,计算298K时0.005mol/kg的CaCl2水溶液中Ca2+和Cl-的活度系数和离子平均活度系数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“根据德拜-休克尔极限定律,计算298K时0.005mol/k…”相关的问题
更多“根据德拜-休克尔极限定律,计算298K时0.005mol/k…”相关的问题
A.z+是指电解质离解出来的阳离子数
B.z是指电解质离解出来的阳离子数
C.z指阴离子的摩尔质量
D.z+是指电解质离解出来的阳离子的电荷数
计算298K时下述电池的电动势E。
Pb(s)|PbCl2(s)|HCl(0.01mol·kg-1)|H2(10kPa)|Pt
已知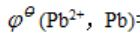 =-0.126V,该温度下PbCl2(s)在水中饱和溶液的浓度为0.039mol·kg-1(用Debye-Huckel极限公式求活度因子后再计算电动势)。
=-0.126V,该温度下PbCl2(s)在水中饱和溶液的浓度为0.039mol·kg-1(用Debye-Huckel极限公式求活度因子后再计算电动势)。
工业生产SO2Cl2(1)有以下两种方法:
SO2(g)+C(g)=SO2Cl2(1)①
SO2(g)+2HCl(g)=SO2Cl2(1)+H2O(1)②
(1)请根据热力学数据计算说明,欲得到更大的转化率,应采用什么路线更好?
(2)对于②反应,增大体系温度,对反应有什么影响?
(3)求反应①在298K时的