 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
已知弱酸NH4+的离解常数为Ka=5.6×10-10,则其共轭碱的pKb()。
A.4.74
B.3.74
C.5.60
D.9.26
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.4.74
B.3.74
C.5.60
D.9.26
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知弱酸NH4+的离解常数为Ka=5.6×10-10,则其共…”相关的问题
更多“已知弱酸NH4+的离解常数为Ka=5.6×10-10,则其共…”相关的问题
度的影响).已知锌氨配离子的各级累积稳定常数为: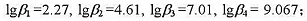 NH4+的离解常数为Ka=10-9.25.
NH4+的离解常数为Ka=10-9.25.
A.NaH2PO4
B.Na2HPO4
C.Na3PO4
D.NaH2PO4+Na2HPO4
A.氨水(Kb=1.8×10-5)
B.苯酚(Kb=1.1×10-10)
C.NH4+
D.H3BO3(Ka=5.8×10-10)
A.5.0×10-5
B.2.0×10-4
C.1.0×10-4
D.A,B,C均不对
试求293K下,混合气体中SO2平衡分压为0.05atm时,SO2在水中的溶解度。已知293K下
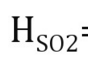 为1.63kmol/(atm·m3),离解常数
为1.63kmol/(atm·m3),离解常数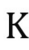 为:
为: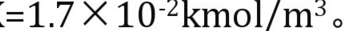
今由某弱酸HB及其盐配制缓冲溶液,其中HB的浓度为0.25mol·L-1。于100mL该缓冲溶液中加入200mgNaOH(忽略溶液体积的变化),所得溶液的pH值为5.60。问原来所配制的缓冲溶液的pH值为多少?(已知HB的Ka=5.0×10-6)
已知Ka(HA)<10-5,HA是很弱的酸,现将α mol·L-1HA溶液加水稀释使溶液的体积为原来的n倍(设α(HA)<<1),下列叙述正确的是()。
A.c(H+)变为原来的1/n
B.HA溶液的离解度增大为原来的n倍
C.c(H+)变为原来的a/n倍
D.c(H+)变为原来的(1/n)1/2
A.苯酚(Kb=1.1×10-10)
B.氨水(Kb=1.8×10-5)
C.H3BO3(Ka=5.8×10-10)
D.NH4+