 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
试计算分解1吨含WO3为65%的黑钨精矿,需投入含NaOH40%的工业液碱多少吨?(碱加量为理论量的1.5倍)
暂无答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试计算分解1吨含WO3为65%的黑钨精矿,需投入含NaOH4…”相关的问题
更多“试计算分解1吨含WO3为65%的黑钨精矿,需投入含NaOH4…”相关的问题
(2)从书中查出上述各碳酸盐的分解温度(CdCO3为345℃),与计算结果加以比较,并加以评价.
(3)各碳酸盐分解温度的实验值与由计算结果所得出的有关碳酸盐的分解温度的规律是否一致?并从离子半径、离子电荷、离子的电子构型等因素对上述规律加以说明.
(3)分解温度的实际值和计算值的规律是一致的.金属离子的半径越小,离子所带的电荷数越大,极化能力就越强,相应碳酸盐分解温度越低;金属离子电子构型为18e的极化能力比8e的强;而极化越大,相应的碳酸盐越易分解.
A.115.2
B.108
C.122.4
D.102
高温下乙酸分解反应如下:
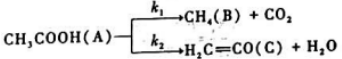
在1089K时,k1=3.74s-1,k2=4.65s-1
(1)试计算乙酸反应掉99%所需的时间;
(2)当乙酸全部分解时,在给定温度下能够获得乙烯酮的最大产量是多少?
要求:请计算本月该铜矿应纳的资源税(三等铜矿单位税额为1.4元/吨)。