 更多“该反应的化学方程式为:4NH3 + 3O2 = 4N + 6…”相关的问题
更多“该反应的化学方程式为:4NH3 + 3O2 = 4N + 6…”相关的问题
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
问题一、选择性催化复原法的脱硝原理为:

①上述反应中每转移3mol电子,生成标准状况下N2的体积为()L。
②已知:2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ•mol-1
N2(g)+3H2(g)=2NH3(g)ΔH=-92.4kJ•mol-1
N2(g)+O2(g)=2NO(g)ΔH=-180.5kJ•mol-1
则反应6NO(g)+4NH3(g)=5N2(g)+6H2O(g)的ΔH=()。
问题二、目前,科学家正在研究一种以乙烯作为复原剂的脱硝(NO)原理,其脱硝机理示意图如以下图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。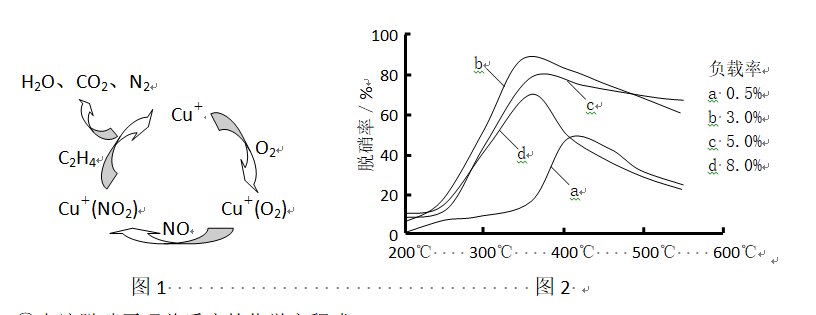
①出该脱硝原理总反应的化学方程式:()。
②为到达最正确脱硝效果,应采取的条件是()。
A.1点
B.2点
C.3点
D.4点
镁是一种用途很广的金属,目前世界上60%的镁是从海水(溶质主要含NaCl和MgCl2等)中提取的,主要步骤如下:
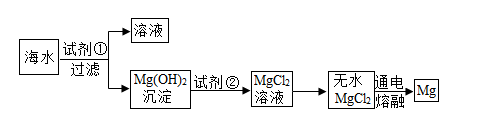
(1)工业生产中,加入试剂①发生反应的化学方程式为() ,试剂②的名称为() ;
(2)写出无水MgCl2在熔融状态下电解制取金属镁的化学方程式 (),该反应属于基本反应类型中的 ()反应。
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
A.ν(O2)=0.01mol/(L·s)
B.ν(NO)=0.008mol/(L·s)
C.ν(H2O)=0.003mol/(L·s)
D.ν(NH3)=0.002mol/(L·s)
A.H2O2分子中含有极性键和非极性键
B.H2O分子中只含极性键
C.H2O2分子中所有原子都达8电子稳定结构
D.该反应中H2O2既是氧化剂也是还原剂
A.该实验可以证明氢氧化钠能与盐酸反应
B.该反应的化学方程式为:HCl + NaOH =NaCl + H2O
C.实验过程中,溶液的pH逐渐增大
D.反应后所得无色溶液的溶质中一定有NaCl,可能有HCl
A.Na2O2是氧化物,其中氧元素化合价为﹣1价
B.R 的化学式为CO2
C.该反应不可以用于实验室制氧气,因为此方法获得的氧气不纯净
D.Na2O2中含有氧分子
工业上用铝土矿(主要成分为氧化铝,含少量氧化铁)制取铝的过程如图所示: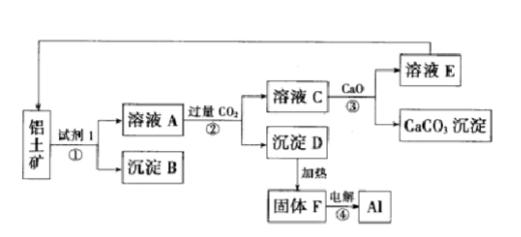 请回答:
请回答:
(1)试剂Ι为()(填化学式),①-④转化中属于氧化还原反应的是()(填序号);
(2)沉淀B的化学式为(),写出该物质发生铝热反应的化学方程式();
(3)电解F,当转移0.6mol,电子时,可制得铝()g;
(4)沉淀D是药物“胃舒平”的主要成分,可用于治疗胃酸(稀盐酸)过多,写出该反应的离子方程式();
(5)②中发生反应的离子方程式为()。


 如果结果不匹配,请
如果结果不匹配,请 

















