 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
CO和H2在一定条件下可合成甲醇CO(g)+2H2(g)CH3OH(g),下列叙述正确的是()。
A.CO和H2可全部转化为甲醇
B.降低体系温度能加快反应速率
C.增大CO浓度能加快反应速率
D.使用催化剂不影响反应速率
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.CO和H2可全部转化为甲醇
B.降低体系温度能加快反应速率
C.增大CO浓度能加快反应速率
D.使用催化剂不影响反应速率
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“CO和H2在一定条件下可合成甲醇CO(g)+2H2(g)CH…”相关的问题
更多“CO和H2在一定条件下可合成甲醇CO(g)+2H2(g)CH…”相关的问题
A.389℃
B.399℃
C.429℃
D.439℃
A.升高温度,反应速度增加
B.升高温度,平衡常数下降
C.增加压力,提高甲醇的平衡产率
D.原料气H2:CO的理论比3∶1
E.适当的空速可提高生产能力,减少副反应
能源是人类共同关注的重要问题。页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)=CO(g)+3H2(g)△H1
已知:①CH4、H2、CO的燃烧热(△H)分别为-a()kJ•mol-1、-bkJ•mol-1、-ckJ•mol-1;②H2O(l)=H2O(g);△H=+dkJ•mol-1
则△H1=()(用含字母a、b、c、d的代数式表示)kJ•mol-1。
(2)用合成气生成甲醇的反应为:CO(g)+2H2(g)⇌CH3OH(g)△H2,在10L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200℃时n(H2)随时间的变化如下表所示:
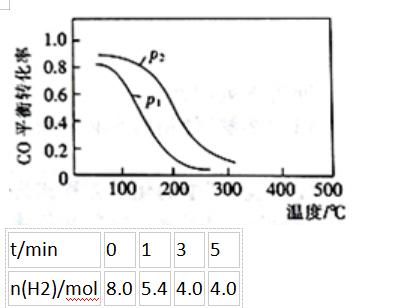 ①△H2()(填“>”“<”或“=”)0。
①△H2()(填“>”“<”或“=”)0。
②下列说法正确的是()(填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
③0〜3min内用CH3OH表示的反应速率v(CH3OH)=()mol•L-1·min-1。(计算结果保留两位有效数字)
④200℃时,该反应的平衡常数K=()。向上述200℃达到平衡的恒容密闭容器中再加入2molCO、2molH2、2molCH3OH,保持温度不变,则化学平衡()(填“正向”、“逆向”或“不”)移动。
(3)甲烷、氧气和KOH溶液可组成燃料电池。标准状况下通入5.6L甲烷,测得电路中转移1.2mol电子,则甲烷的利用率为()。