 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
容器中放有CO2和N2,温度为25℃,其分压均为1bar,则xco2 =() ,xN2=() 。
容器中放有CO2和N2,温度为25℃,其分压均为1bar,则xco2=() ,xN2=() 。
容器中放有CO2和N2,温度为25℃,其分压均为1bar,则xco2=() ,xN2=() 。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
容器中放有CO2和N2,温度为25℃,其分压均为1bar,则xco2=() ,xN2=() 。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“容器中放有CO2和N2,温度为25℃,其分压均为1bar,则…”相关的问题
更多“容器中放有CO2和N2,温度为25℃,其分压均为1bar,则…”相关的问题
(1)保持容器内温度恒定抽去隔板,计算气体混合后的压力;
(2)分别计算混合气体中H2和 N2的分压;
(3)分别计算混合气体中H2和N2的分体积.
血氧饱和度的大小主要决定于()
A.血中Hb含量多少
B.血中P(N2)大小
C.血中P(CO2)大小
D.血中P(O2)大小
E.血液温度高低
在一密闭容器中进行如下反应:C(s)+O2(g)====CO2(g),下列说法错误的是( )。
(A) 将木炭粉碎成粉末状可以加快化学反应速率
(B) 升高温度可以加快化学反应速率
(C) 增加O2的分压可以加快化学反应速率
(D) 增加木炭的量可以加快化学反应速率
A.3,2
B.3,1
C.1,0
D.2,1
某温度下对合成氨反应速率测得如下数据:Ac(NH3)/△t=2.0×10-4mol.L-1.s-1;如果以-△c(N2)/△t表示反应速率,其值为________________mol.L-1.s-1;若以一△c(H2)/t表示反应速率,则为________________mol.L-1.s-1。
硝基乙酸在酸性溶液中的分解反应
(NO2)CH2COOH(1)→CH3NO2(I)+CO2(g)
为一级反应.25℃,101.3kPa下,测定不同反应时间产生的CO2(g)体积如下:
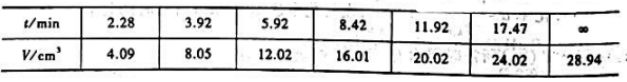
反应不是从t=0开始的.求速率常数k.