 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算pH=10.0,CNH3=0.1mol·L-1Zn2+/Zn的溶液中电对的条件电极电位(忽略离子强
计算pH=10.0,CNH3=0.1mol·L-1Zn2+/Zn的溶液中电对的条件电极电位(忽略离子强
度的影响).已知锌氨配离子的各级累积稳定常数为: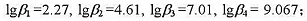 NH4+的离解常数为Ka=10-9.25.
NH4+的离解常数为Ka=10-9.25.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“计算pH=10.0,CNH3=0.1mol·L-1Zn2+/…”相关的问题
更多“计算pH=10.0,CNH3=0.1mol·L-1Zn2+/…”相关的问题
 为2.0、5.0、7.0、10.0; M(OH)42+的
为2.0、5.0、7.0、10.0; M(OH)42+的 试计算0.10mol-1·L-1HCOONH4溶液的pH。
试计算0.10mol-1·L-1HCOONH4溶液的pH。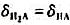 ;当pH=6.22时,
;当pH=6.22时,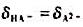 。计算:①H2A的pKa1和pKa2;②当溶液中的主要存在型体为HA-时,溶液的pH。
。计算:①H2A的pKa1和pKa2;②当溶液中的主要存在型体为HA-时,溶液的pH。
















