 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
气相反应SO2CI2(g)→SO2(g)+CI2(g)在320℃时的速半常数k=2.2x10-5s-1.问在320℃加热90min时SO2CI2(g)的分解分数α为多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“气相反应SO2CI2(g)→SO2(g)+CI2(g)在32…”相关的问题
更多“气相反应SO2CI2(g)→SO2(g)+CI2(g)在32…”相关的问题
考虑以下反应


由SO2(g)和O2(g)所生成的SO3(g)的量是在高温增加还是在低温增加?
工业生产SO2Cl2(1)有以下两种方法:
SO2(g)+C(g)=SO2Cl2(1)①
SO2(g)+2HCl(g)=SO2Cl2(1)+H2O(1)②
(1)请根据热力学数据计算说明,欲得到更大的转化率,应采用什么路线更好?
(2)对于②反应,增大体系温度,对反应有什么影响?
(3)求反应①在298K时的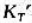
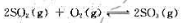
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
dP(mm) | 3.175 | 6.35 | 9.525 |
R【mol/(s·g(cat))】 | 4.85×10-4 | 4.01×10-4 | 3.54×10-4 |
为了减少固定床反应器的压降,克服粒内阻力,希望采用的最大颗粒直径为多少?
已知
(忽略热效应影响,反应能保证在50℃进行)
杂质,过滤后得到溶液B.将某非金属单质C加入溶液B中加热,反应后再经过滤、除杂等过程后,得溶液D.取3mL溶液D加入HCI溶液,其反应产物之一为沉淀C.另取3mL溶液D,加入少许AgBr(s),则其溶解,生成配离子E.再取第3份3mL溶液D,在其中加入几滴溴水,溴水颜色消失,再加入BaCl2溶液,得到不溶解于稀盐酸的白色沉淀F.试确定A、B、C、D、E、F的化学式,并写出各步反应方程式.
根据Le Chatelier原理,讨论下列反应:
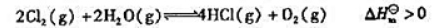
将Cl2,H2O(g),HCl(g),O2四种气休混合后,反应达到平衡时,下列左面的操作条件改变对右面各物理鼠的平衡数值有何影响(操作条件中没有注明的,是指温度不变和体积不变)?

今有含SO2的空气需要净化处理。采用以活性炭为催化剂,以水为液体介质的滴流床反应器,在0.101MPa,25℃下将SO2氧化为SO3,溶于水而成稀硫酸从反应器底部流出。反应的控制步骤是O2在催化剂表面的吸附,以O2表示的反应速率
rA=ηρPkcAS[mol/(cm3·s)](按床层体积计)
式中,cAS为催化剂表面处的O2浓度,单位为mol/cm3。已知:内扩散有效因子η=0.6,堆密度ρb=1.0g/cm3,1级反应速率常数k=0.06cm3/(g·s),床层空隙率ε=0.3,kLSaS=0.3s-1,kLaL=0.03s-1,气体流量为100cm3/s,O2在水中溶解度的亨利常数H=5.0,反应器直径10cm,塔顶入口处气体的摩尔分数分别为SO22%,O219%,N279%。试求SO2转化率为80%时滴流床反应器的床层高度。
估算在400K,101.325kPa下汽相混合物的平衡组成(以摩尔分数表示),该气体含有正戊烷、异戊烷和新戊烷异构体。在400K下反应的标准生成热数据为:
5C(s)+6H2(g)====n-C5H12(g) △Gf=40.195kJ·mol-1
5C(s)+6H2(g)====i-C5H12(g) △Gf=34.415kJ·mol-1
5C(s)+6H2(g)====n-C5H12(g) △Gf=37.640kJ·mol-1
已知:(1)S(单斜,s)+O2(g)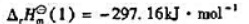
S(正交,5)+O2(g)→+SO2(B)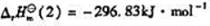
计算S(单斜,s)→+S(正交,)的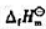 并判断单斜硫和正交硫何者更稳定.
并判断单斜硫和正交硫何者更稳定.