 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
设在某一溶液中有两种物资,在反应开始时,两种物资的量分别为a和b;又设在时刻t,两种物资已经起反
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“设在某一溶液中有两种物资,在反应开始时,两种物资的量分别为a…”相关的问题
更多“设在某一溶液中有两种物资,在反应开始时,两种物资的量分别为a…”相关的问题
A.HY一定是弱酸
B.酸性HX>HY
C.HX一定是强酸
D.反应开始时二者生成H2的速率相同
实验室里可用甲醇等有关物质制备HCHO,关于甲醇和甲醛的沸点和水溶性见下表: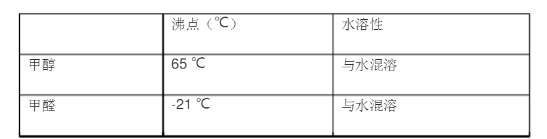 某校化学兴趣小组的甲、乙两位同学,在研究性学习中,运用以上信息和已有知识分别设计了二套实验室制取HCHO装置,如图甲和乙。
某校化学兴趣小组的甲、乙两位同学,在研究性学习中,运用以上信息和已有知识分别设计了二套实验室制取HCHO装置,如图甲和乙。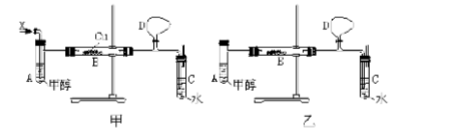
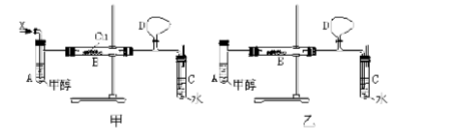 据此请你回答下列问题:
据此请你回答下列问题:
(1)若按甲装置进行实验,则通入A试管的X应是();B中反应的化学方程式是()。
(2)若按乙装置进行实验,则B管中应装入()。
(3)当实验完成时,若在C中滴加适量银氨溶液,并用水浴将C加热,发生反应的化学方程式是()。
(4)在反应过程中,甲、乙两种装置中都需直接加热的仪器是()(填A、B、C)。
(5)实验开始时,先打开气球D的开关,直至实验结束。气球D的作用是()。
(6)从生成甲醛的产量来看,你认为两套装置中较好的是()(填“甲”或“乙”)。
在298K时,测定乙酸乙酯皂化反应速率。反应开始时,溶液中酯和碱的浓度都为0.01mol·dm-3,每隔一定时间,用标准酸溶液滴定其中的碱含量,实验所得结果如下:
| t/min | 3 | 5 | 7 | 10 | 15 | 2l | 25 |
| OH-/(10-3mol·dm-3) | 7.40 | 6.34 | 5.50 | 4.64 | 3.63 | 2.88 | 2.54 |

在298 K时,测定乙酸乙酯皂化反应速率。反应开始时,溶液中酯和碱的浓度都为0.01mol·dm-3,每隔一定时间,用标准酸溶液滴定其中的碱含量,实验所得结果如下:

(1)证明该反应为二级反应,并求出速率常数k值;
(2)若酯和碱的起始浓度都为0.002mol·dm-3,试计算该反应完成95%时所需的时间及该反应的半衰期。
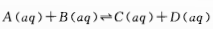 开始时只有A和B,经长时间反应,最终结果是()。
开始时只有A和B,经长时间反应,最终结果是()。A.C和D的浓度大于A和B的浓度
B. A和B的浓度大于C和D的浓度
C. A、B、C、D的浓度不再变化
D. A、B、C、D浓度相等
蔗糖在稀硫酸溶液中按照下式进行水解:
C12H22O11+H2O→C6H12O6(葡萄糖)+C6H12O6(果糖)
当温度与酸的浓度一定时,反应速率与蔗糖的浓度成正比。今有一溶液,1dm3中含0.300molC12H22O11及0.1molHCl,在48℃时,20min内有x(C12H22O11)=0.32的C12H22O11水解。(1)计算反应速率系(常)数;(2)计算反应开始时(t=0)及20min时的反应速率;(3)问40min后有多少蔗糖水解?
A.滤渣中一定有铜,可能有铁和镁
B.滤液中一定有锌离子和镁离子,可能有铁离子、铜离子
C.向滤渣中加稀盐酸,有气泡冒出,则滤液一定无色
D.若滤渣中只有两种单质,则一定是铜和铁
E.反应后溶液的质量可能变大
F.若滤渣中有三种金属单质,则滤液中的溶质只有硝酸锌和硝酸镁
A.10ml 2mol/L Na2S2O3 + 10ml 2mol/LHCl
B.10ml 4mol/lLNa2S2O3 + 30ml 1.2 mol/LHCl
C.10ml 1mol/L Na2S2O3 + 30ml 0.5mol/LHCl
D.10ml 1mol/L Na2S2O3 + 30ml 1 mol/LHCl
A.加入有色布条,有色布条褪色,说明原溶液中有Cl2存在
B.溶液呈黄绿色,且有刺激性气味,说明有Cl2分子存在
C.加入盐酸酸化的AgNO3溶液产生白色沉淀,说明原溶液中有Cl-存在
D.加入NaOH溶液,氯水黄绿色消失,说明原溶液中有HClO分子存在