 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一定条件下的反应C(s)+H2O(g)⇌CO(g)+H2(g)ΔH>0,达到平衡后下列叙述正确的是()
A.减小压强,平衡正向移动
B.加入固体碳,平衡正向移动
C.加入水蒸气,平衡不移动
D.升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
 答案
答案
A、减小压强,平衡正向移动
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.减小压强,平衡正向移动
B.加入固体碳,平衡正向移动
C.加入水蒸气,平衡不移动
D.升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
 答案
答案
A、减小压强,平衡正向移动
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“一定条件下的反应C(s)+H2O(g)⇌CO(g)+H2(g…”相关的问题
更多“一定条件下的反应C(s)+H2O(g)⇌CO(g)+H2(g…”相关的问题
A.反应CH4(g)+H2O(g)═CO(g)+3H2(g)在一定条件下能自发进行,该反应一定为放热反应
B.可用牺牲阳极或外加电流的阴极保护法延缓钢铁水闸的腐蚀
C.Na2O2与水反应产生1molO2,理论上转移的电子数目约为4×6.02×1023
D.保持温度不变,向稀氨水中缓慢通入CO2,溶液中c(OH-)/c(NH3•H2O)的值增大
A.生成1molCO的同时生成1molH2
B.容器中物质的总质量不发生变化
C.n(H2O):n(H2)=1 :1
D.v逆(H2O)=v正(CO)
)和CO2(g)。当该分解反应达到平衡后,系统中共有压力不变的条件下将平衡系统中Na2CO3(s)除去·部分,化学平衡衡系统中的NaHCO3(s)全部除去,在其他条件不变时系统处于()。
A.①②③④
B.①③④
C.①②
D.①③
A.①③
B.①④
C.②③
D.③④
A.该反应中熵变、焓变皆大于0
B.该反应是吸热反应,因此一定不能自发进行
C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定能自发进行
D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应
已知在温度为298.15K的标准条件下,CO(g)和H2O(g)的标准摩尔生成焓分别为-110.53kJ/mol和-241.83kJ/mol。计算反应H2O(g)+C(石墨)====CO(g)+H2(g)的标准摩尔焓变。
A.在平衡混合物中 c(CO):c(CO2) = 2:1
B.碳和二氧化碳不再化合,一氧化碳不再分解
C.单位时间内,若消耗 n mol二氧化碳,同时消耗 n mol碳
D.平衡时,若条件不变,则二氧化碳和一氧化碳的浓度不变
已知在298K时,下列反应:
①CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s),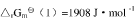
②
③C(石墨)+O2(g)===CO2(g),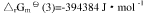
④N2(g)+3H2(g)===2NH3(g),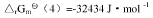 试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能
试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能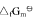 ;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数
;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数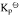 。
。