 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知: C(s)+O2(g)=CO2(g) △Hθ =-393.5kJ·mol-1 Mg(s)+ O2(g)=MgO(s) △Hθ =-601.8kJ·mol-1 Mg(s)+C(s)+ O2(g)=MgCO3(s) △Hθ =-1113kJ·mol-1 则 MgO(s)+CO2(g)=MgCO3(s)的 △Hθ为()kJ·mol-1
A.-235.4
B.-58.85
C.-117.7
D.-1321
 答案
答案
C、-117.7
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“已知: C(s)+O2(g)=CO2(g) △Hθ =-39…”相关的问题
更多“已知: C(s)+O2(g)=CO2(g) △Hθ =-39…”相关的问题
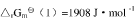

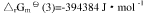
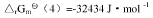 试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能
试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能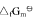 ;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数
;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数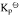 。
。 。
。 =-1246.2kJ·mol-1
=-1246.2kJ·mol-1 =+90.9kJ·mol-1
=+90.9kJ·mol-1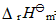 =+483.6kJ·mol-1
=+483.6kJ·mol-1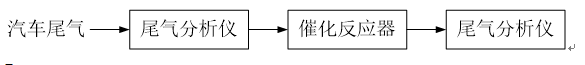
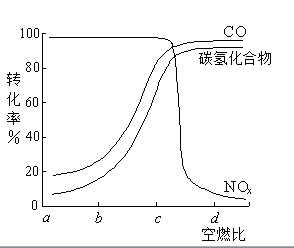
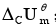 (3)C10H8(s)的
(3)C10H8(s)的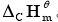 。
。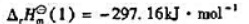
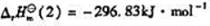
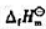 并判断单斜硫和正交硫何者更稳定.
并判断单斜硫和正交硫何者更稳定.
















